- 25
- 14
- ♥ 收藏
- A大中小
资本市场有一句名言,存在即合理。
很多朋友认为港股君实生物市值只有400+亿港币,A股的君实1500亿市值则是高估的。这是犯了以偏概全的错误。
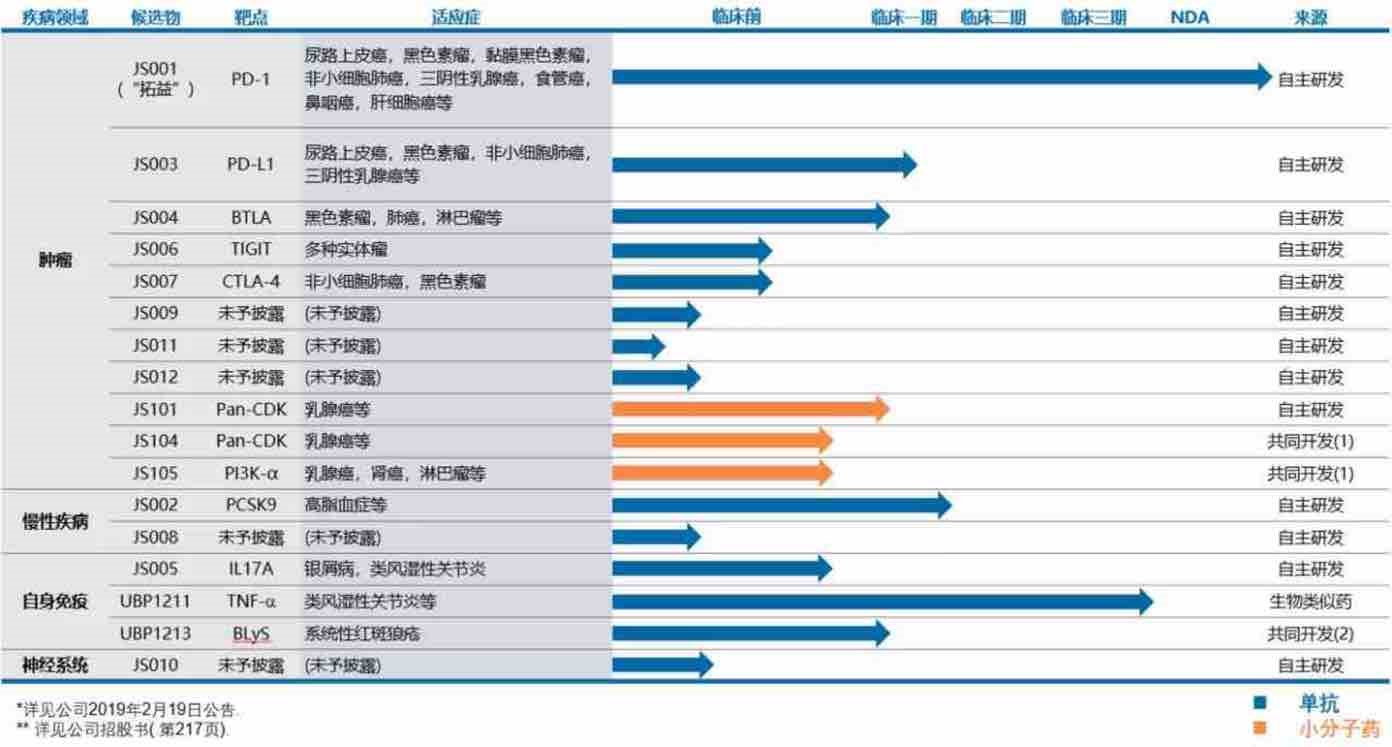
(1)对比A股2价HPV疫苗的万泰生物,甘精胰岛素生物类似药的甘李药业均超过了1000亿市值。君实生物(A股)在研全球领先的新冠中和抗体,无疑需要给予500亿市值加分。
【2020年,公司与中科院微生物所以及跨国药企礼来联合开展新冠中和抗体JS016的研发合作,并于6月相继获得国家药监局以及 FDA 的 IND 批准,成为全球第一个进入临床试验的新冠中和抗体品种。】
JS016 为公司与中国科学院微生物研究所合作开发新型冠状病毒中和抗体,双方已就此签订技术转让(专利申请技术实施许可)合同。中国科学院微 生物研究所以“2019 新型冠状病毒抗体”应用领域独占方式许可君实生物实施其所拥有的相关专利/专利申请,用于 2019 新型冠状病毒抗体的开发。君 实生物及其关联方在全球范围内独家拥有在许可专利申请技术基础上进行 2019 新型冠状病毒抗体新药研发、生产和商业化的权益;中国科学院微生物研究所应向君实生物提交与许可专利申请技术有关的技术资料,提供技术服务和技术指导。君实生物向中国科学院微生物研究所支付许可专利申请技术使用费。
对疫苗,民众的理解有三大误区:
第一,搞不明白疫苗和特效药的区别。一听说疫苗的研发如何如何,就觉得躺在医院里的那些感染者有救了。
其实不然,通俗来讲,疫苗的作用是预防,是用到健康人身上的,特效药的作用是治疗,是用到病人身上的!
第二,不了解从进入临床试验到民众可以大规模接种这中间的过程和距离。一听说临床试验有效果就觉得每人扎一针大家就都安全了。
所以相对于药物,疫苗的临床试验要求更高,审批也更为严格,从研发开始,真正通过能够严格按照国家标准,通过I/II/III期临床,再审批进入市场,中间的路程很长很长,少则几年多则十来年都是可能的,具体请参考国产HPV疫苗和乙肝疫苗。
而且,国内目前的疫情控制较好,III期临床大概率要去国外做了,这中间也会涉及到更多的问题。
所以,非特殊情况,非特殊群体,在没有完成临床试验和审批之前,是绝对不会冒着风险在健康人身上接种新冠疫苗的。
第三,产能,从研发到生产,多大的工厂,多大的产能,满足多少人的接种需求,是否符合GMP标准,这也不是一天或者两天就能解决的。
流感疫苗每年都在生产,接种的群体也仅建议老人、小孩等免疫力较低的人群,但是每年都是一苗难求,基本都是处于供不应求的状态,试想,民众大规模接种,是个什级别,需要多少工厂多大产能才能生产出来?
但可喜的是,在新冠疫苗的自主研发和生产方面,我国是走在世界最前列的,各项进展也都非常顺利,如果万一有疫情大面积爆发的情况,我们也是有武器去对抗的。
目前最主要的三种疫苗分别是:
第一:重组新型冠状病毒疫苗
由军事科学院军事医学研究院生物工程研究所联合开发的(Ad5-nCoV),是最早进入临床实验的疫苗,II期临床试验已于6月11日揭盲完成,目前已获批在军队内部使用;由中科院微生物所和安徽智飞龙科马生物共同研发的重组苗,目前已获批进入I期临床试验。
第二,新冠灭活疫苗
中国生物武汉生物制品研究所研发的新冠灭活疫苗,于4月12日全球首家进入Ⅰ/Ⅱ期临床试验;由国药集团中国生物研发的新冠灭活疫苗,已于6月23与阿联酋阿布扎比签署了相关临床合作协议,标志着全球首个新冠灭活疫苗国际临床试验(Ⅲ期)正式启动。
第三,新冠mRNA疫苗
由苏州艾博生物科技有限公司联合军事科学院军事医学研究院、云南沃森生物技术股份有限公司共同研制的新型冠状病毒mRNA疫苗(ARCoV)于6月19日获批进入临床试验,也是我国第一个获批进入临床试验的mRNA疫苗。
另外,除了用于预防的疫苗以外,用于治疗新冠的中和抗体类药物的研发也在快速推进。
6月7日君实生物宣布,其与中国科学院微生物研究所共同开发的重组全人源抗SARS-CoV-2单克隆抗体注射液获批进入I期临床试验阶段,在复旦大学附属华山医院完成首例受试者给药。
这是全球首个在健康受试者中开展的新冠病毒中和抗体临床试验,也是国内最早进入临床阶段的新冠病毒中和抗体。
对于新冠肺炎这种自限性疾病来说,只要病人能挺过最危险的时期,直到自身产生结合病毒的抗体,就能够痊愈。所以保证病人存活最关键的地方在于怎么样让病人不会在中途因为过于剧烈的免疫反应,呼吸困难而死亡。注射中和抗体,即使不能完全清除病毒,只要能降低病毒载量,防止病人进入重症,平稳地撑到痊愈,对于新冠这样的疾病其实已经足够了。另外抗体是人源化的蛋白,相对来说会安全一些。目前临床实验已经开展,具体效果如何得等到临床实验之后才能确认。也可能会跟其它课题组研发出的抗体一起组成鸡尾酒来提高疗效。
(2)港股信达生物-B的估值已经高达700亿港币,而支撑其估值的正是——买来的PD-1单价(信迪利单抗)。信达的PD-1单抗,每年却要和礼来平分营收,请注意不是平分利润。
这样折算下来,信达生物(H股)真实估值=1400亿港币。信达生物盈利时间节点更晚,大致6年时间内不会在A股IPO上市。
(3)PD-1单抗的竞争,是适应症研发速度的竞争。
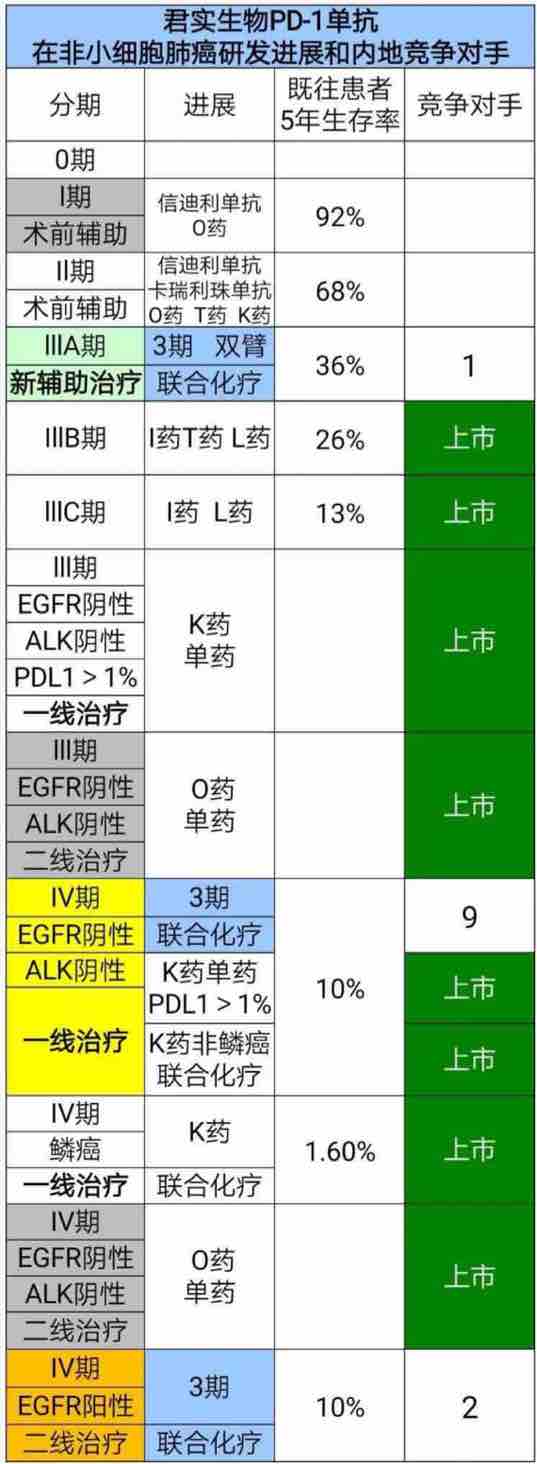
PD-1单抗最大的适应症是肺恶性肿瘤。
君实生物的PD-1单抗(特瑞普利单抗)在肺恶性肿瘤开发了三个适应症(均已启动3期临床)。
EGFR阴性lllA期非小细胞肺癌的手术后新辅助治疗,君实的竞争对手只有复宏汉霖。
由于PD-1单抗使用有惯性,患者首先使用了君实的,即使未来疾病进展了,也不会再使用恒瑞的了。
EGFR阳性Ⅳ期非小细胞肺癌二线治疗,君实的竞争对手只有恒瑞医药和信达生物。
EGFR阴性lV期非小细胞肺癌的一线治疗,君实生物也在参与竞争,竞争对手共有9家,是红海。
所以,君实生物可能在未来的肺癌适应症应用人群中,占据最大的市场份额。
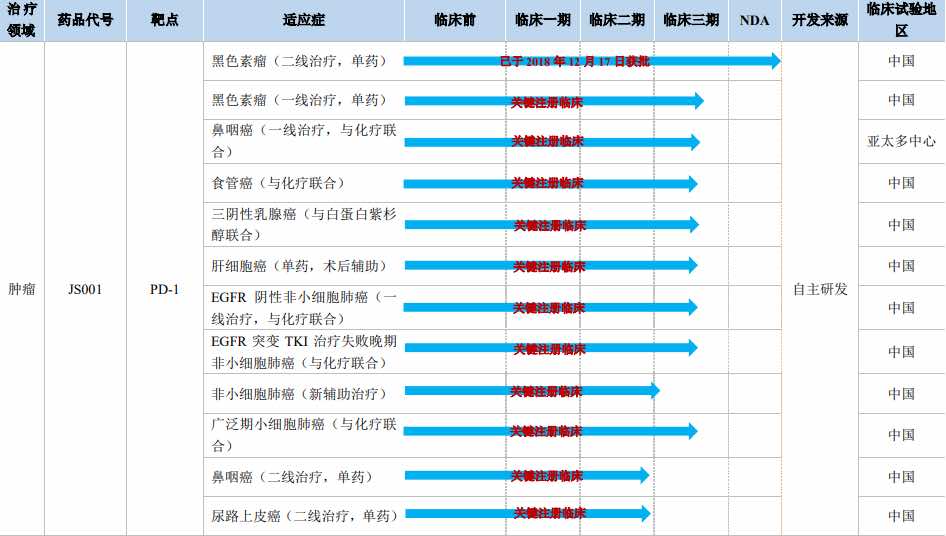
(4)君实生物(H股)没有纳入港股通,不能享受流动性溢价。低估是非常合理的。
(5)君实生物(A股)大概率成为科创板指数成分股,100亿市值,尚不够ETF指数基金填牙缝。


