- 3
- 评论
- ♥ 收藏
- A大中小
今日(12月19日),中国国家药监局药品审评中心(CDE)官网公示,百济神州申报的1类新药注射用BG-C137获批临床,拟开发用于晚期实体瘤患者。公开资料显示,BG-C137是一款靶向FGFR2b的抗体偶联药物(ADC),百济神州拟开发该产品用于上消化道瘤种和乳腺癌。根据CDE官网查询,本次为该产品首次在中国获批临床。
截图来源:CDE官网
FGFR2b是在胃和皮肤等部位上皮细胞中发现的FGF受体的一种形式,大约在30%的HER2阴性胃食管癌患者中过度表达。阻断FGFR2b的激活被认为会延缓癌症的进展。
百济神州公开资料介绍,该公司研发的靶向FGFR2b的ADC具有差异化抗体骨架,有效载荷为拓扑异构酶I抑制剂,DAR为8。该产品具有旁观者效应,可解决肿瘤异质性问题;此外其配体阻断作用较弱,因此不会产生靶向角膜毒性。临床前数据也显示其在小鼠中不产生角膜毒性。
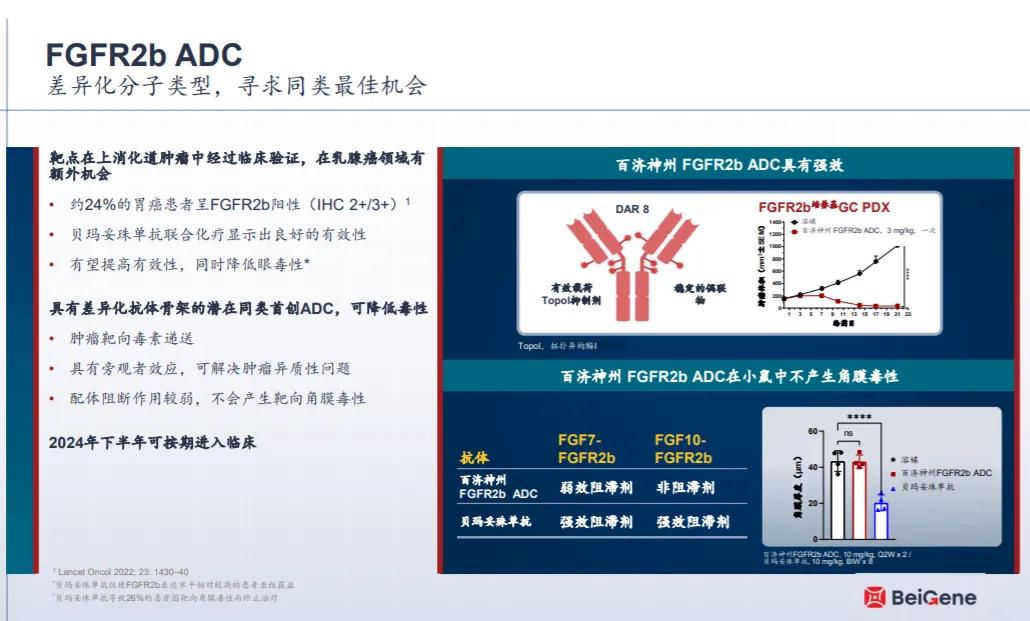
截图来源:百济神州第三季度投资者演示材料
根据ClinicalTrials官网,百济神州已经于今年12月在美国开启BG-C137的1a/b期临床研究,本研究的目的是评估BG-C137在晚期实体瘤患者中的安全性、耐受性、药代动力学(PK)、药效学和初步抗肿瘤活性。本次该产品在中国获批临床,意味着其也将在中国进入临床开发阶段。
根据百济神州公开资料,该公司2024年已经有超过10个新分子实体(NME)进入临床。尤其是11月以来,该公司多款新药陆续获批临床,包括BG-T187(EGFR/MET三特异性抗体)、BG-C477(靶向CEA的ADC)、BGB-58067(PRMT5抑制剂)。此外,新型EGFR降解剂(EGFR CDAC)BG-60366片临床试验申请已经获得CDE受理,也有望在2024年进入临床阶段。
$百济神州(HK|06160)$$恒生医疗ETF(SH513060)$$上证指数(SH000001)$#商务部将加快出台首发经济政策文件#
来源:医药观澜
免责声明:转载内容仅供读者参考,版权归原作者所有,内容为作者个人观点,不代表其任职机构立场及任何产品的投资策略。本文只提供参考并不构成任何投资及应用建议。如您认为本文对您的知识产权造成了侵害,请立即告知,我们将在第一时间处理。
(来源:恒生医疗ETF的财富号 2024-12-20 15:19) [点击查看原文]


